尋夢新聞LINE@每日推播熱門推薦文章,趣聞不漏接❤️
每經編輯:彭水萍
據新華社,美國食品和藥物管理局(FDA)22日批准首款可緊急用於治療新冠病毒感染的口服藥物,用於治療患新冠輕症至中症的成人和12歲及以上兒童,以及具有較高重症風險的人群。另據央視新聞,經美國食品藥品監督管理局的審查,輝瑞生產的口服藥目前的適合人群為12歲及以上、體重不低於40公斤的患者。

圖片來源:每日經濟新聞 資料圖
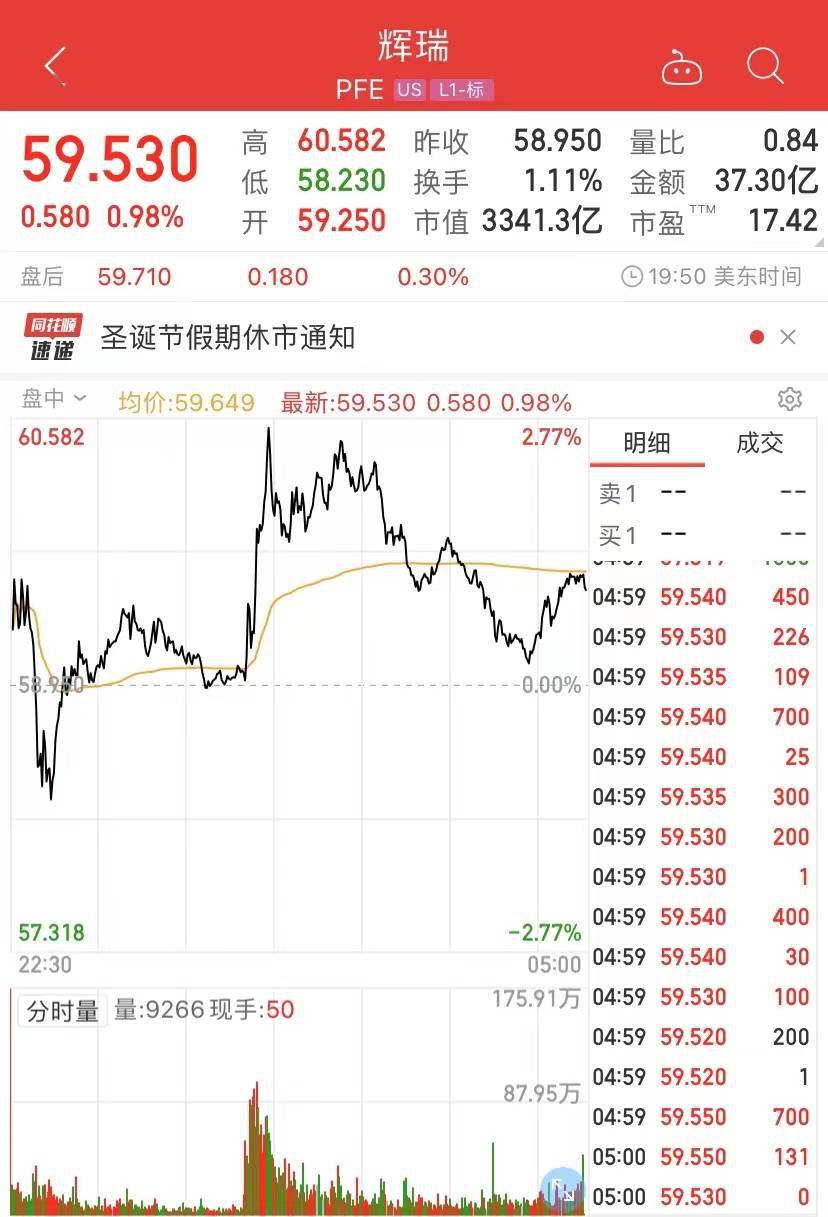
受此消息提振,輝瑞股價收漲約0.98%,盤中一度上漲近3%。
據新華社,美藥管局在一份聲明中說,美國輝瑞公司生產的這款口服藥物名為Paxlovid,由兩種抗病毒藥物組成。患者須在確診新冠後盡快服用,並在出現新冠症狀後5天內開始服用,連續使用時間不能超過5天。
聲明說,經過對所有可用科學依據的評估,美藥管局認為Paxlovid可能對治療新冠輕症至中症患者有效,其已知和潛在益處超過其已知和潛在風險。這款藥物的常見副作用可能包括味覺受損、腹瀉、高血壓和肌肉酸痛等。
展開全文
美藥管局藥物評估和研究中心主任卡瓦佐尼表示,隨著新變異毒株的出現,新冠疫情防控進入關鍵階段,緊急授權使用這款口服藥物為抗擊新冠病毒提供了新的工具。
據新華社此前消息,歐洲藥品管理局12月16日發布公告,建議歐盟成員國在緊急情況下可使用尚未在歐盟獲得授權的美國輝瑞公司新冠口服藥PAXLOVID。根據公告,該藥物可用於治療不需要輔助供氧但病情發展成重症風險較高的成年新冠患者,患者應在確診感染且症狀出現後5天內服藥。
據紅星新聞援引外媒11月5日報導,輝瑞稱其研發的新冠口服藥可將高危新冠患者的住院和死亡風險降低89%。公司在一份聲明中表示,「由於療效驚人」,將不再招募新患者進行臨床試驗,並計劃盡快將研究結果提交給美國監藥物管機構以獲得緊急使用授權。
輝瑞當時稱,對1219名嚴重疾病患病風險較高、且未接種疫苗的成年新冠患者進行試驗,在症狀出現後3~5天內使用輝瑞口服藥進行為期5天的治療,結果顯示住院率明顯降低,只有0.8%的患者住院,並且沒有人死亡。而在此窗口期使用安慰劑的人中,有7%的人住院且有7人死亡。
輝瑞的臨床試驗結果意味著,人們在新冠感染早期有兩種口服藥使用選擇,來防止病情加重。外媒稱,從公布的數據看,輝瑞的優勢要超過默沙東的新冠口服藥莫努匹韋(「molnupiravir」),後者能夠將輕度至中度新冠患者的重病或死亡風險降50%。10月,默沙東制藥公司與合作夥伴Ridgeback Biotherapeutics向美國藥監局提交了口服藥的授權申請,11月還未通過,但已於11月4日在英國已獲得批准。這也是全球面世的首款抗新冠口服藥物。
據報導,輝瑞這款名為Paxlovid的口服藥可阻斷新冠病毒復制時所需的一種關鍵酶,阻止病毒自我復制。而除了目前在高危新冠患者中進行的試驗外,輝瑞正在探索這種藥物是否可以用作預防藥物,防止暴露在病毒下的人感染新冠。
輝瑞發言人表示,預計到2021年底將生產超過18萬份口服藥,到明年年底前生產5000萬份。並計劃採用差別定價,在中、高收入國傢的定價將比低收入國傢高,但目前還沒有給出明確的價格。
來源:每日經濟新聞綜合新華社、央視新聞、紅星新聞
每日經濟新聞
